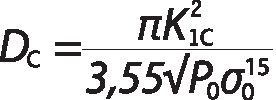Podczas procesu produkcji szkła płaskiego istnieje możliwość pojawienia się w uformowanej tafli szklanej defektu w postaci inkluzji siarczku niklu. Zjawisko to zaobserwowano po raz pierwszy w 1960 roku.
Mimo, że wtrącenia siarczku niklu zdarzają się bardzo rzadko dla typowego szkła krzemianowo-sodowo-wapniowych (SLS) w ilości 5 μg na tonę (średnia koncentracja 5 cząstek na 1012 kg), nadal ich eliminacja pozostaje nie rozwiązanym problemem.
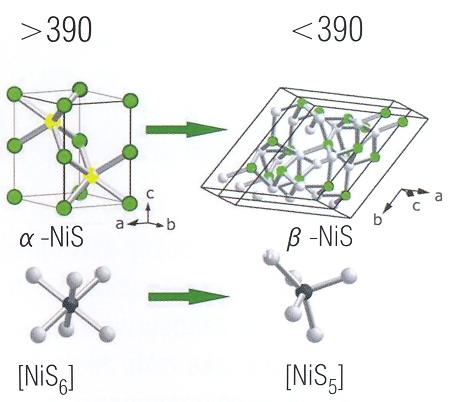
Siarczek niklu jest krystalicznym związkiem polimorficznym, występującym w dwóch odmianach alotropowych, wysoko i niskotemperaturowej. Niskotemperaturowa faza α-NiS jest trwała poniżej 390°C, natomiast wysokotemperaturowa faza β-NiS powyżej tej temperatury [1].
Takie wtrącenia są niegroźne, jeżeli tafle szkła, w których one występują, nie są przeznaczone do procesu hartowania. Problem pojawia się, gdy tafla z wtrąceniem siarczku niklu zostaje zahartowana, czyli poddana obróbce termicznej w celu wytworzenia charakterystycznego układu naprężeń, powodujących wzrost wytrzymałości mechanicznej i termicznej [2].
Hartowanie polega na podgrzaniu szkła do możliwie wysokiej temperatury a następnie na szybkim jego studzeniu.
Gorące szkło w pierwszym okresie energicznego studzenia dmuchawą powietrzną podlega następującym przemianom:
. w pierwszym etapie następuje gwałtowny skurcz warstw wierzchnich, które tracą swą ciągliwość i ściskają wewnętrzne warstwy gorącego szkła. W tym okresie powstają w warstwach zewnętrznych naprężenia rozrywające, a w wewnętrznych – ściskające.
. w drugim etapie hartowania następuje odwrócenie naprężeń (inwersja). Szkło części środkowej stygnie dalej, lecz nie może się kurczyć prawidłowo, gdyż przeszkadza temu zewnętrzna, sztywna już skorupa. To powoduje, że w przedmiocie zahartowanym warstwy wewnętrzne mają naprężenia rozrywające, a zewnętrzne -ściskające. Jednocześnie objętość przedmiotu zahartowanego się nie zmniejsza. Czas inwersji naprężeń zależy od intensywności chłodzenia i właściwości cieplnych szkła [3, 4].
Występujący w takiej tafli szklanej siarczek niklu zostaje „zamrożony” w formie wysokotemperaturowej, która charakteryzuje się mniejszą objętością niż forma niskotemperaturowa. Wysokotemperaturowa forma α-NiS jest metastabilną fazą w temperaturze otoczenia i dąży do przemiany w stabilną w tej temperaturze formę β-NiS.
Podczas tej przemiany następuje znaczący wzrost objętości. Proces ten jest znacznie rozciągnięty w czasie i może spowodować pęknięcie szkła nawet po kilku latach jego użytkowania. Jest to bardzo niebezpieczne zjawisko, gdyż szyba z pozoru pozbawiona jakichkolwiek wad po pewnym czasie ulega pęknięciu, na skutek przekroczenia dopuszczalnych naprężeń.
Szczególnie duże prawdopodobieństwo zniszczenia szyby występuje, jeżeli cząsteczka siarczku niklu występuje w strefie naprężeń rozciągających, ponieważ szkło jest nawet ośmiokrotnie bardziej wytrzymałe na naprężenia ściskające niż na naprężenia rozciągające [4].
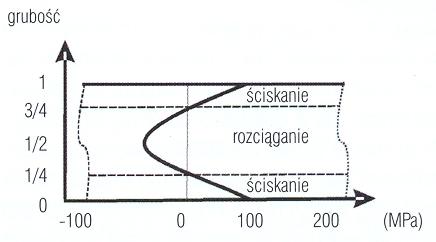
Szkło ma dość wysoki moduł Younga 70 000 MPa (porównywalny z aluminium) oraz wysoką wytrzymałość na ściskanie 800-1000 MPa Wytrzymałość szkła na zginanie oraz na rozciąganie jest znacznie niższa i wynosi 30-90 MPa. Niezwykle istotnym parametrem mającym wpływ na spontaniczne pęknięcie szkła hartowanego pod wpływem NiS jest jego położenie w tafli szklanego panelu.
Na rysunku 1 przedstawiono rozkład naprężeń panelu szklanego. Jeżeli inkluzja NiS będzie występowała w strefie naprężeń ściskających, zmiana objętości odmiany wysokotemperaturowej α-NiS w formę β-NiS, będzie powstrzymana i nie zainicjuje pęknięcia. Natomiast, podczas gdy inkluzja NiS będzie występowała w strefie naprężeń rozciągających, wzrost objętości, który towarzyszy przejściu formy α-NiS w β-NiS oraz zmiany rozszerzalności termicznej spowodują pogorszenie stabilności struktury szkła, zainicjują mikro defekt prowadzący do pęknięcia.

Kolejnym parametrem mającym wpływ na zjawisko spontanicznego pęknięcia szkła pod wpływem NiS jest rozmiar inkluzji. Na podstawie mechanicznego modelu naprężeń występującego dookoła sferycznej inkluzji stwierdzono, że istnieje krytyczna wartość średnicy inkluzji Dc, przy której następuje pęknięcie. Jej wartość zależna jest od naprężeń wewnętrznych σ0, oraz stopnia zahartowania szkła.
|
Wyliczona teoretycznie wartość minimalna średnicy inkluzji NiS prowadząca do spontanicznego pęknięcia szkła – 50 μm, w praktyce przyjmuje się 60 μm. |
W świetle danych literaturowych w szkle mogą występować różne typy wtrąceń siarczku niklu. Według Tabuchi istnieją trzy różne typy wtrąceń siarczku niklu w szkle. Pierwszy i drugi typ Ni3S2 wtrąceń siarczku niklu nie powoduje spontanicznego pękania szkieł hartowanych, natomiast związek o składzie zbliżonym do NiS, może być przyczyną spontanicznego pękania tafli szklanych.
Na podstawie prowadzonych badań wykazano, że zakres składu niebezpiecznych wtrąceń siarczku niklu mieści się w granicach od Ni7S6 do NiS1.03. Wtrącenia te jednak nie składają się ściśle z pojedynczej fazy, ale mogą zawierać kilka faz takich jak: Ni7S6, Ni9S8 i Ni1-xSx [5].
Wtrącenia siarczku niklu nie wykazują termodynamicznej stabilności w masie szklanej, dlatego nie ma możliwości ich tworzenia w stopie. Siarczek niklu w zasadzie jest nierozpuszczalny w szkle, jednak warunki utleniające panujące podczas topienia szkła krzemianowo-wapniowo-sodowego wpływają na jego utlenianie do tlenku niklu. Tlenek niklu natomiast jest dobrze rozpuszczalny w masie szklanej, toteż następuje jego szybki rozkład [6].
Na podstawie prowadzonych przez Kaspera i Stadelmanna badań stwierdzono, że przebieg reakcji tworzenia siarczku niklu jest kilkuetapowy. Poprzez dodatek do masy szklanej drobnych cząsteczek stali hartowanej mniej szlachetne metale, jak chrom i mangan, uległy rozpuszczeniu w szkle, tym samym skład chemiczny stali uległ pewnej zmianie (utworzył się stop żelazo-nikiel). Na skutek postępu reakcji żelazo zostało usunięte pozostawiając metaliczny nikiel. W trzeciej fazie reakcji metaliczny nikiel reagował z siarką tworząc związek typu Ni3S2.
Dopóki w masie występował metaliczny nikiel, związek typu Ni3S2 był fazą stabilną. Po zużyciu metalicznego niklu, wtrącenia siarczku niklu w kontakcie z masą szklaną uległy powolnemu rozkładowi, z utworzeniem na ich powierzchni rozpuszczalnego tlenku niklu. Równocześnie inkluzje Ni3S2 utraciły nikiel z utworzeniem fazy NiS. Kasper i Stadelmann wykazali, że siarczek niklu może pozostać jako metastabilna faza w szkle w obecności metalicznego niklu. Występuje więc konieczność unikania kontaktu między stopami niklu a surowcami wykorzystywanymi do produkcji szkła krzemianowo-wapniowo-sodowego [7].
Wtrącenia NiS mogą być wtrąceniami polikrystalicznymi i składać się z kilku krystalicznych faz siarczku niklu, różniących się składem chemicznym, np.: Ni7S6, Ni3S2, Ni1-xSx, Ni2S3.
Temperatura przemiany formy α → β zmienia się w zależności od zawartości siarki w siarczku niklu [8].
W kryształach siarczku niklu może występować różne stężenie Fe, co jest ściśle uzależnione od zawartości żelaza w szkle. We wtrąceniach i porach pomiędzy kryształami NiS, wykryto występowanie znaczącej ilości żelaza [8].
Właściwości i charakterystyka siarczku niklu NiS.
Dwiema dobrze poznanymi formami siarczku niklu (II) są wysokotemperaturowa heksagonalna faza α-NiS i niskotemperaturowa trygonalna forma β-NiS (ileryt). ileryt jest minerałem niklu, często występującym z innymi ważnymi rudami tj: żelazowo-niklową lub żelazowo-miedziową.
Charakteryzuje się wysokim przewodnictwem elektrycznym (przewodnictwo metaliczne) i prawdopodobnie posiada strukturę diamagnetyczną. Przeprowadzono wiele badań nad fazą α-NiS ze względu na charakterystyczne przejście metal → półprzewodnik w temperaturze 265 K.
Zainteresowanie α-NiS było również spowodowane możliwością jego zastosowania jako niklowego analogu pirytu Fe1-xS, który w temperaturze powyżej 883 K tworzy roztwór stały pomiędzy Fe i Ni, tzw. „siarczkowy roztwór stały”.
Wysokotemperaturowa faza α-NiS, posiada heksagonalną strukturę typu NiAs, która jest fazą metastabilną w warunkach otoczenia, niespotykaną w naturze.
Kullerud i Yund stwierdzili, że forma β-NiS (ileryt) ulega transformacji do formy wysokotemperaturowej w temperaturze 652 K, przy ciśnieniu atmosferycznym [9].
W znacznym stopniu na temperaturę przejścia formy α → β ma wpływ ciśnienie. Przy wzroście ciśnienia obserwuje się gwałtowny spadek temperatury przemiany Tα → β. W warunkach ciśnienia atmosferycznego przemiana fazowa związana jest również ze wzrostem objętości o 2,8% [10].
Ten wzrost objętości może doprowadzić do spontanicznego pękania szyb hartowanych zawierających nawet drobne wtrącenia NiS.
Przemiana α → β pociąga za sobą znaczną reorganizację struktury oraz zmianę liczby koordynacyjnej z LK=6 (dla formy wysokotemperaturowej) na LK=5 (dla formy niskotemperaturowej, rys. 3).
Ponieważ faza α-NiS posiada dużo szerszy zakres stechiometryczny niż niskotemperaturowa faza β-NiS, dlatego skład równowagowy faz α i β-NiS zależy od kierunku przemiany. Podczas przemiany fazy β → α, cała faza β przechodzi w fazę α bez żadnej zmiany w budowie.
Przejście fazy ubogiej w nikiel α-Ni1-xSx do fazy β-NiS związane jest z roztworzeniem α-Ni1-xSx [10].
Przemiana α → β dla fazy ubogiej w nikiel α-Ni1-xSx staje się wolniejsza w miarę zwiększania niedoboru niklu w porównaniu ze składem stechiometrycznym α-NiS [12].
Równomolowy α-NiS ulega transformacji do fazy β w ciągu kilkunastu minut w temperaturze 523 K, podczas gdy transformacja fazy ubogiej w nikiel α-Ni0,93S, jest o dwa rzędy wielkości wolniejsza. Kullerud i Yund (1962) stwierdzili, że przemiana α-NiS / α-Ni1-xSx → β-NiS jest egzotermicznym, samorzutnym procesem w niskich temperaturach, jednak bardzo powolnym w temperaturze 298 K.
Wtrącenia bliskie składowi stechiometrycznemu NiS mogą być najbardziej niebezpieczne w szkle hartowanym, natomiast niestechiometryczne wtrącenia mogą tak długo ulegać transformacji, że nie doprowadzą do zniszczenia szkła [6].
Możliwe reakcje prowadzące do utworzenia siarczku niklu w szkle
Fazą stabilną w warunkach panujących w agregatach topliwnych mógłby być Ni3S2, pod warunkiem występowania atmosfery redukcyjnej. Prawdopodobnie Ni3S2 musi tworzyć się w masie szklanej, a faza NiS formuje się dopiero w części wyrobowej lub czasie formowania. Sam mechanizm przemiany Ni3S2 w NiS nie jest do końca poznany. Aktualnie proponowane są następujące reakcje tworzenia NiS [8].
a) Pierwszy mechanizm tworzenia NiS w szkle:
Ni3S2 + Na2SO4 + 1" C → 3NiS + Na2O + 1" CO2
Reakcja ta byłaby prawdziwa pod warunkiem wprowadzania do zestawu związków: siarczanu (VI) sodu i węgla. Związki te są wprowadzane z sulfatem, stosowanym jako środek klarujący oraz grafitem lub koksikiem, wprowadzanym w celu opóźnienia rozkładu temperaturowego sulfatu. We wtrąceniu po transformacji musiałby występować tlenek sodu. Za tym mechanizmem transformacji przemawia pojawianie się węgla w przebadanych wtrąceniach.
Natomiast przeciwko tej reakcji przemawia niewielka zawartość tlenku sodu na powierzchni wtrąceń. Małe jest także prawdopodobieństwo, że Ni3S2 spotka się z Na2SO4 i C w czasie wypływania masy szklanej z basenu topliwnego na kąpiel cynową.
b) Drugi mechanizm przemiany Ni3S2 do NiS:
Kolejny mechanizm jest opisywany jako proces dwuetapowy. Pierwszy etap jest związany z reakcjami przebiegającymi w basenie topliwnym, natomiast drugi z reakcjami zachodzącymi w części wyrobowej.
I etap:
3NiO + 2Na2SO4 + 3C → Ni3S2 + 2Na2O + 3CO2
Część tlenku sodu może rozpuścić się w szkle, więc tylko część tego tlenku występuje we wtrąceniach.
II etap:
2Ni3S2 + 2S2 → 6NiS
W czasie chłodzenia szkła na kąpieli cynowej wtrącenia mogą być dodatkowo wzbogacane w siarkę, która była rozpuszczona w szkle.
Autorzy twierdzą, że ta reakcja jest możliwa ze względu na dużą szybkość reakcji oraz krótki czas przebywania szkła na kąpieli cynowej [8, 13].
Możliwe źródła pojawiania się siarczku niklu w masie szklanej.
Temperatura topienia siarczku niklu wynosi około 850ºC, dlatego też istnieją podejrzenia, iż związek ten może syntezować się w czasie produkcji szkła płaskiego metodą float.
Pochodzenie siarki w masie szklanej jest ogólnie znane, dodawana jest ona do zestawu głównie w postaci Na2SO4 (sulfat) jako środek klarujący. Ponadto siarka znajduje się w samym gazie używanym do opalania agregatu topliwnego.
Natomiast pochodzenie niklu nie jest do końca znane, głównie ze względu na znaczną liczbę potencjalnych źródeł jego uwalniania. Analizując budowę linii produkcyjnej do produkcji szkła płaskiego możemy zauważyć, że silosy do przechowywania surowców, wagi do naważania surowców, mieszadła, zasypniki, palniki, mieszadła, obudowy aparatury pomiarowej oraz chłodnice zbudowane są ze stali zawierającej nikiel. Stale te mimo dużej odporności na działanie środowisk korozyjnych, w wysokich temperaturach nie są odporne na działanie siarki. Prowadzi to do tworzenia się na powierzchni takich stali produktów siarczkowych, między innymi siarczku niklu.
Kolejnym źródłem uwalniania niklu mogą być materiały ogniotrwałe, które w wyniku korozyjnego oddziaływania masy szklanej i wysokiej temperatury dostają się do stopionego zestawu. Badania składu chemicznego oleju opałowego używanego do opalania pieców topliwnych wykazały, że zawiera on śladowe ilości niklu.
Zastąpienie oleju opałowego gazem ziemnym oraz użycie zasypników i lepszych palników z lepszych jakościowo materiałów poprawia sytuację, ale nie rozwiązuje problemu związanego z samoistnym pękaniem szkieł hartowanych [2].
Trudnym do wyeliminowania źródłem niklu może okazać się stłuczka szklana pochodząca ze szkieł pokrywanych miękkimi powłokami magnetronowymi. Powłoki te składają się z kilku napylonych na szkło warstw, między innymi z cienkiej warstwy niklu.
Metody redukcji inkluzji NiS w szkłach wzmacnianych termicznie i hartowanych
Wystąpienie wtrąceń siarczku niklu NiS może być eliminowane na poziomie procesu technologicznego poprzez dodatek do szklistego stopu związków Zn, tj (ZnSO47H2O) czy (Zn(NO3)26H2O).
Z uwagi na panujące podczas topienia warunki utleniające-redukcyjne dodatek niektórych tlenków metali, związków żelaza czy azotanów również wpływa na redukcję wtrąceń NiS. Przy pomocy HTS redukcja wtrąceń NiS, których wymiary są mniejsze od 20 mikrometrów, nie jest możliwa.
Metody zapobiegające spontanicznym pęknięciom szkła na skutek inkluzji NiS:
1. Dodatek związków cynku do stopionego szkła może zredukować wtrącenia NiS mniejsze od 20 µm. Metoda ta jest bardzo efektywna i mało kosztowna. Związki Zn w szkłach krzemianowo-sodowo-wapniowych (SLS) są łatwo identyfikowane poprzez metody analizy chemicznej.
2. Kontrola warunków ulteniająco-redukcyjnych podczas procesu topienia, by nie dopuścić do powstania inkluzji.
3. HST z uwzględnieniem kinetyki przejść odmiany wysokotemperaturowej α w odmianę niskotemperaturową β kilku typów związków siarczku niklu tj. NiS, Ni1-xSx, czy Ni7S6, itp.
M. Reben, J. Wasylak, M. Szumiński
AGH, Kraków
S. Bielecki
Huta Szkła „Ewa”, Tarnów
Literatura
1. G. Kullerud, R.A. Yund: The Ni-S system and related minerals, “Journal of Petrology”, 126-175, 1962.
2. J. Wasylak, S. Bielecki: Zjawisko spontanicznego pękania użytkowego szkła hartowanego wywołane obecnością siarczku niklu. „Ceramika”, vol. 103, 2008, Kraków.
3. M. Drajewicz, M. Reben, K. Cholewa-Kowalska: Zmiana budowy wewnętrznej szkła – hartowanie i odprężanie, „Świat Szkła”, 6 (109) Czerwiec 2007, Warszawa.
4. W. Nowotny: Technologia szkła. Część II, PWSZ, Warszawa, 210-212, 1985.
5. Tabuchi: On the study of sulfide inclusions in plate glasses, Proc. 10th International Congress on Glass, Kyoto, vol. 3, 54-58, 1974.
6. L. Merker: Behavior of nickel sulfide in glass. “Glasteschnishe Berichte“, vol.47, 116.121, 1974.
7. A. Kasper, H. Stadelmann: Chemical behaviour of nickel sulfide in soda-lime-silica glass melts, “Glass Science and Technology”, vol. 75, 1-11, 2002.
8. C. Barry, S. Ford: An electron microscopic study of nickel sulphide inclusions in toghened glass, “J. Materials Science”, vol. 36, 3721-3730, 2001.
9. G. Kullerud, R.A. Yund: The Ni-S system and related minerals, “Journal of Petrology”, 126-175, 1962.
10. H. Wang, A. Pring, Y. Ngothai, B. O’Neill: The kinetics of the α → β transition in synthetic nickel monosulfide, “American Mineralogist”, vol. 91, 171-181, 2006.
11. M. Reben, J. Wasylak, S. Bielecki: Spontaniczne pękanie szkła hartowanego stosowanego w budownictwie, Materiały konferencyjne 55 Konferencji Naukowej Komitetu Inżynierii Lądowej i Wodnej PAN i Komitetu Nauki PZITB, Krynica 2009.
12. S.R. Krishnakumar, N. Shanthi, D.D. Sarma: Electronic structure of millerite NiS “Physical Review”, B66, 115105-115110, 2002.
13. A. Kasper, S. Moschek, H. Stadelman, R. Zeihe: Composition and structure of NiS inclusions in Float Glass, and their impact on the Heat Soak Process, Glass Processing Days, 2003.
patrz też:
- Inkluzje siarczku niklu jako wada szkła hartowanego Część 3 , Manuela Reben, Sebastian Bielecki, Świat Szkła 2/2016
- Inkluzje siarczku niklu jako wada szkła hartowanego Część 2 , Manuela Reben, Sebastian Bielecki, Świat Szkła 1/2015
- Inkluzje siarczku niklu jako wada szkła hartowanego Część 1 , Manuela Reben, Sebastian Bielecki, Świat Szkła 5/2014
- Wady szkła na fasadach Część 1 Szkło hartowane i warstwowe, Anna Balon-Wróbel, Agnieszka Marczewska, Świat Szkła 3/2012
- Oszklenia bezpieczne w budownictwie , Tadeusz Tarczoń, Świat Szkła 10/2010
- Inkluzje siarczku niklu w szkle , M. Reben, J. Wasylak, M. Szumiński, S. Bielecki, Świat Szkła 1/2010
- Poprawa właściwości fizykochemicznych szkła float, Marcin Drajewicz , Jan Wasylak, Świat Szkła 12/2008
- Zmiana budowy wewnętrznej szkła – hartowanie i odprężanie, Marcin Drajewicz, Manuela Reben, Katarzyna Cholewa-Kowalska, Świat Szkła 6/2007
- Uszlachetnianie powierzchni szkła , Jan Wasylak, Marcin Drajewicz, Świat Szkła 12/2006
Całość artykułu w wydaniu drukowanym i elektronicznym
inne artykuły o podobnej tematyce patrz Serwisy Tematyczne
więcej informacji: Świat Szkła 1/2010